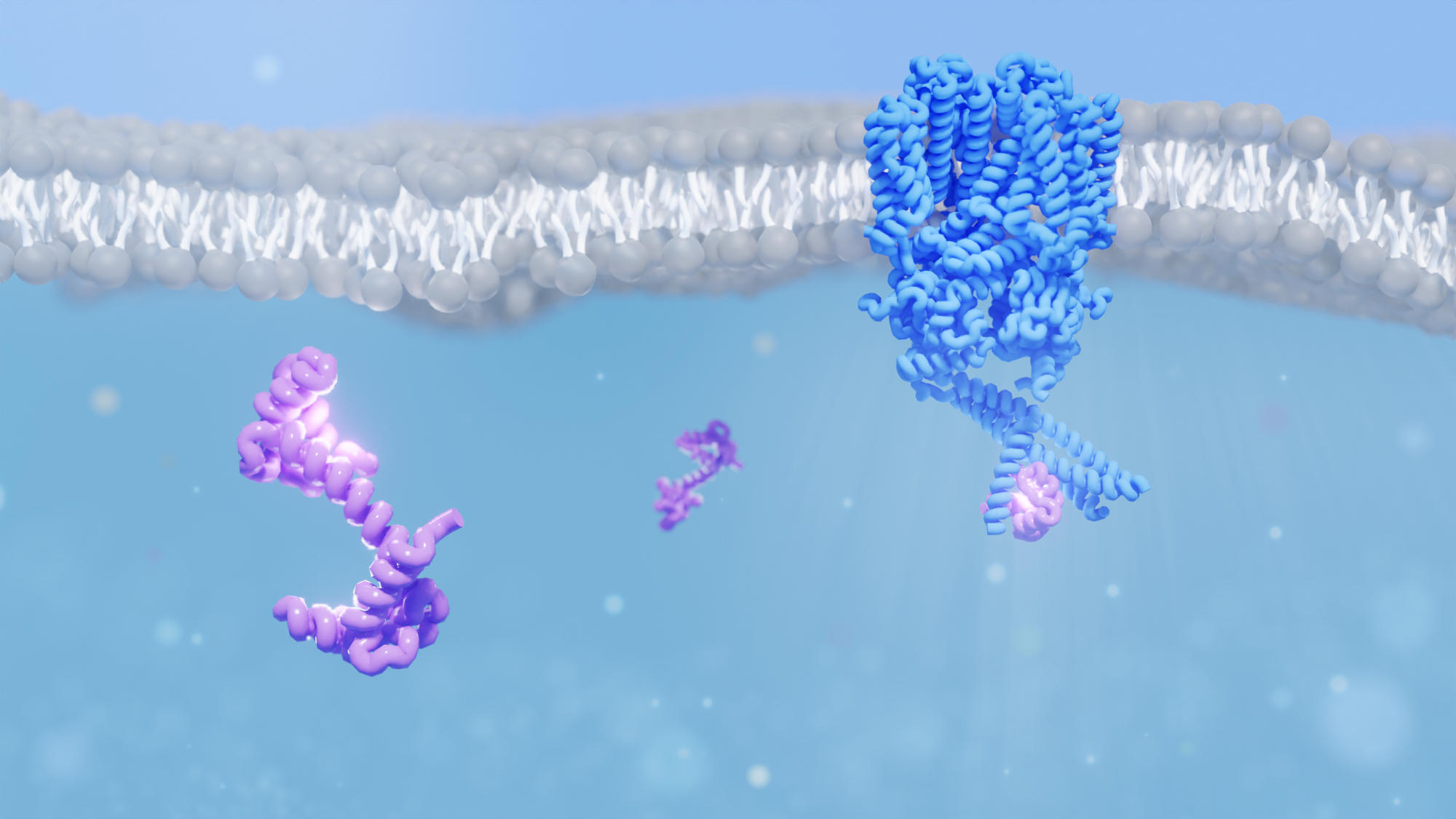
لقد فهم الباحثون بنية القناة الأيونية من الخلايا العصوية للعين (الموضحة باللون الأزرق) عندما تتفاعل مع بروتين كالودولين (أرجواني). هذا التفاعل مهم لوظيفة القناة الأيونية في العين ، ولكن أيضًا لوظيفة القناة الأيونية في أجزاء أخرى من الجسم ، مثل القلب. الائتمان: شركة بول شيرير / تينا شوستر
سلطت النتائج الجديدة المثيرة الضوء على التفاعلات بين بروتين كالودولين وقناة أيونية في العين ، مما يكشف السر وراء حساسية أعيننا الاستثنائية لظروف الإضاءة المنخفضة.
باستخدام الفحص المجهري للإلكترون بالتبريد وقياس الطيف الكتلي ، نجح فريق من الباحثين في PSI في الكشف عن بنية قناة أيونية في العين تتفاعل مع بروتين الهدودولين ، وهو لغز حير العلماء لمدة 30 عامًا. قد يفسر هذا الارتباط كيف يمكن لأعيننا تحقيق مثل هذه الحساسية الملحوظة للضوء الخافت. تم نشر النتائج في المجلة PNAS.
عندما تنظر إلى شاشة ساطعة على هاتفك أو جهاز الكمبيوتر ، فإن القنوات الأيونية في عينيك تتفاعل مع الضوء من خلال إغلاقها. يمثل هذا الإجراء ذروة تفاعل كيميائي متسلسل بدأه التعرض للضوء. نتيجة لذلك ، لم يعد بإمكان أيونات الكالسيوم المرور عبر القنوات الموجودة في غشاء الخلية ، مما يؤدي إلى تحويل الإشارة البيوكيميائية إلى كهرباء. تنتقل هذه الإشارة بعد ذلك عبر الجهاز العصبي وتصل في النهاية إلى عقلك للمعالجة.
تحدث نفس العملية عندما تقف بالخارج ليلاً وتنظر إلى السماء. الآن ، تقوم الخلايا العصوية بالخدعة. هذه هي الخلايا التي تحسس أعيننا لمستويات منخفضة من الضوء ، مما يمكننا من رؤية سماء الليل واكتشاف عدد قليل من فوتونات الضوء من نجم بعيد. نحن نأخذ هذا كأمر مسلم به ، لكنه إنجاز رائع.
قام الآن فريق بقيادة عالم PSI جاكوبو مارينو بتطوير فهمنا لكيفية مساعدة بروتين صغير يسمى كالموديولين في تحقيق ذلك من خلال التفاعل مع القنوات الأيونية في الخلايا السلكية. Calmodulin هو جهاز استشعار للكالسيوم. إنها إحدى آليات الاتصال العالمية للخلية – حيث تساعد الخلية على الاستجابة لتقلبات الكالسيوم. قامت هذه المجموعة ، بالتعاون بين مجموعات في PSI و ETH Zurich و University of Bonn ، بتوضيح البنية ثلاثية الأبعاد لقناة أيون ذات بوابات نيوكليوتيد دائرية (CNG) مع ارتباط بالكالودولين.
وظيفة هامة للكالودولين في العين
قبل عام ، نجح الباحثون في فهم بنية هذه القناة الأيونية نفسها ، والتي توجد في الخلايا العصوية لشبكية عين البقرة والتي تشبه القناة الأيونية الموجودة في الخلايا العصوية في أعيننا. يتكون Rod CNG من أربع وحدات فرعية مشتركة مع العديد من القنوات الأيونية. الميزة الفريدة للقناة ، مع ذلك ، هي أن ثلاث وحدات فرعية ، تسمى الوحدة الفرعية A ، متطابقة ، في حين أن الوحدة الفرعية الرابعة – الوحدة الفرعية B – مختلفة.
لقد عرف العلماء منذ فترة طويلة أن هذه الوحدة الفرعية تربط الكالمودولين. تظهر هذه الميزة في جميع أنحاء مملكة الحيوان. ومع ذلك ، فإن الطبيعة الدقيقة لدورها لا تزال غير واضحة. يوضح مارينو: “إذا تم الحفاظ على شيء ما من خلال التطور ، فهذا مؤشر قوي جدًا على أنه مهم بطريقة ما”. “نحن نعلم أن الهدودولين يعدل نشاط القناة من خلال الوحدة الفرعية B ، ولكن نوع التغييرات الهيكلية التي تحدث ظل لغزًا كبيرًا منذ حوالي ثلاثين عامًا ، ويرجع ذلك أساسًا إلى أن الناس لم يتمكنوا من حل بنية القناة الأيونية.”
الآن ، يمكن للباحثين تقديم رؤية ثلاثية الأبعاد لما يحدث بالفعل. من خلال مزيج من الفحص المجهري الإلكتروني بالتبريد وقياس الطيف الكتلي ، تمكنوا من ملاحظة أن القناة الأيونية تصبح أكثر إحكاما بقليل عندما يرتبط الكالمودولين.
يعتقد الباحثون أن هذه طريقة الطبيعة لإبقاء القنوات مغلقة. ماذا سيكون الغرض من هذا؟ يقول مارينو: “نعتقد أن هذه طريقة لتقليل فتحات القنوات التلقائية التي تسبب ضوضاء في الخلفية ، حتى تتمكن أعيننا من إدراك الضوء الخافت”.
يساعد قياس الطيف الكتلي الباحثين على حل بنية منحنية
ليس من السهل اشتقاق بنية كالمودولين وربط القناة الأيونية. يحدث التفاعل بين الكالمودولين والقضيب CNG في الجزء الأكثر مرونة من القناة ، حيث يتذبذب بحرية. في المجهر الإلكتروني بالتبريد ، يجعل هذا الحصول على معلومات هيكلية عالية الدقة أمرًا صعبًا للغاية. هنا ، يقدم مارينو تشبيهًا ، “تخيل أن لديك غرفة رقص. تلتقط صورة وتريد معرفة شكل جسم الإنسان منها. يمكنك معرفة شكل الرأس ، لكن تحريك الأطراف في كل مكان سيؤدي إلى طمس الساقين والذراعين.
بفضل اجتماع فرصة ، تمكن الفريق من تضييق نطاق هذا الإطار الرشيق. دكتوراه. استمعت الطالبة تينا شوستر إلى شرح مارينو. يتذكر قائلاً: “كنا مستعدين للنشر استنادًا إلى بيانات الفحص المجهري للإلكترون بالتبريد وحدها ، والتي تركت معظم التفاعلات غامضة ، واقتربت مني دينا وقالت ،” أعتقد أنني أستطيع مساعدتك “.
يقوم شوستر بتطوير تقنيات جديدة قائمة على قياس الطيف الكتلي لدراسة تفاعلات البروتين. تستخدم هذه التقنيات الإنزيمات لتقطيع البروتينات إلى أجزاء أثناء ارتباطها كيميائيًا أو داخل أجزاء من غشاء الشبكية. يتم تحديد شظايا البروتين ، التي يرتبط بعضها ببعضها البعض ، عن طريق قياس الطيف الكتلي. يكشف هذا عن معلومات حول أجزاء البروتين التي كانت قريبة من بعضها البعض في فضاء ثلاثي الأبعاد – أقرب إلى تجميع أحجية ثلاثية الأبعاد معًا. يوضح شوستر ، المؤلف الأول المشترك للنشر مع طالبة الدكتوراه ديان باريت: “سمحت لنا هذه التقنيات بتضييق نطاق بعض الاحتمالات التي يحجبها الفحص المجهري الإلكتروني بالتبريد”.
من عجائب الرؤية إلى الآثار المترتبة على صحة الإنسان
ينظم Calmodulin القنوات الأيونية ليس فقط في العين ولكن في جميع أنحاء الجسم ، ويتحكم في الإشارات الكهربائية الضرورية للتشغيل السليم للعضلات والأعضاء المختلفة. في السنوات الأخيرة ، عندما يحدث خطأ في هذا الاتصال بسبب الطفرات في جين الكودودولين ، يمكن أن تحدث آثار صحية خطيرة مثل قصور القلب: شيء لا يزال غير مفهوم تمامًا.
قد تساعد النتائج والأساليب المستخدمة في هذه الدراسة في فهمنا لتفاعلات الكالمودولين مع القنوات الأيونية في أجزاء أخرى من الجسم ، بالإضافة إلى مساعدتنا في فهم معجزة أساسية للغاية.
المرجع: Diane CA Barrett، Tina Schuster، Matthew J. رودريغيز ، ألكسندر ليتنر ، باولا بيجوتي ، جيبهاردت إف إكس شيرتلر ، يو. بنيامين كوب ، فولوديميكوف ، فولوديميروف ، ديان سي. جاكوبو مارينو ، 3 أبريل 2023 ، وقائع الأكاديمية الوطنية للعلوم.
DOI: 10.1073 / pnas.2300309120